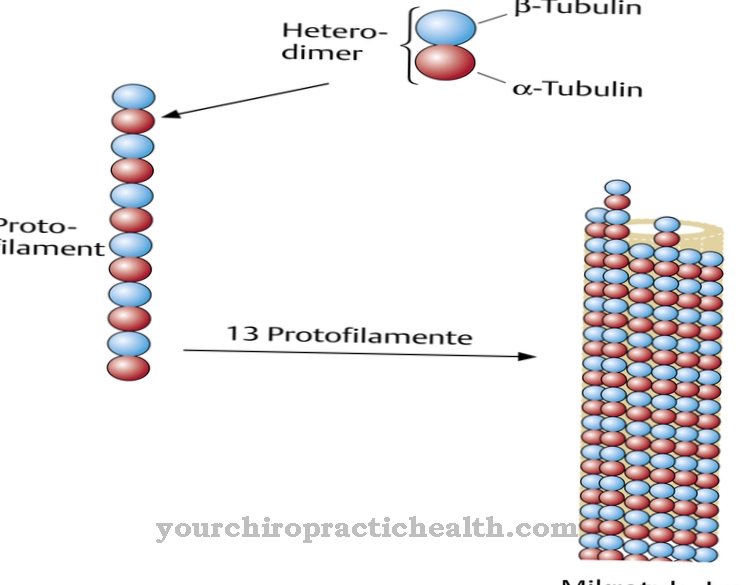
Itu Ikatan hidrogen merupakan interaksi antar molekul yang menyerupai interaksi Van der Waals dan terjadi dalam tubuh manusia. Ikatan tersebut berperan terutama sehubungan dengan ikatan peptida dan rantai asam amino dalam protein. Tanpa kemampuan untuk berikatan dengan ikatan hidrogen, suatu organisme tidak dapat hidup karena kekurangan asam amino penting.
Apa ikatan hidrogennya?

Ikatan hidrogen disebut Ikatan hidrogen atau H jembatan disingkat. Ini adalah efek kimiawi yang berhubungan dengan interaksi menarik atom hidrogen yang terikat secara kovalen dengan pasangan elektron bebas dari atom pengelompokan atom. Interaksi tersebut didasarkan pada polaritas dan, dijelaskan lebih tepatnya, terdiri antara atom hidrogen yang terpolarisasi secara positif dalam gugus amino atau hidroksil dan pasangan elektron bebas dalam gugus fungsi lain.
Interaksi hanya terjadi dalam keadaan tertentu. Salah satu syaratnya adalah sifat elektronegatif dari pasangan elektron bebas. Properti ini harus lebih kuat dari properti elektronegatif hidrogen untuk membuat ikatan yang kuat. Atom hidrogen dengan demikian dapat terikat menjadi kutub. Atom yang bebas secara elektronegatif dapat berupa nitrogen, oksigen, dan fluor, misalnya.
Ikatan hidrogen adalah ikatan valensi sekunder, yang kekuatannya biasanya jauh di bawah ikatan kovalen atau ikatan ionik. Molekul dalam ikatan hidrogen memiliki titik leleh yang relatif tinggi dan titik didih yang sama tinggi terkait dengan massa molar mereka. Ikatan memiliki relevansi medis terutama dalam kaitannya dengan peptida dan asam nukleat dalam suatu organisme.
Ikatan hidrogen adalah gaya antarmolekul. Tanpa keberadaannya, air tidak akan ada di berbagai keadaan agregat, tetapi akan berbentuk gas.
Fungsi & tugas
Ikatan hidrogen hanya memiliki interaksi yang lemah dan terjadi antara dua partikel atau di dalam molekul. Dalam konteks ini, jenis ikatan berperan, misalnya untuk pembentukan struktur tersier pada protein. Dalam biokimia, struktur protein berarti tingkat struktural protein atau peptida yang berbeda. Struktur zat yang terjadi secara alami ini secara hierarkis dibagi menjadi struktur primer, struktur sekunder, struktur tersier, dan struktur kuaterner.
Urutan asam amino adalah struktur utama. Kapanpun protein disebutkan dalam kaitannya dengan pengaturan spasialnya, konformasi protein dan fenomena perubahan konformasi sering dirujuk. Dalam konteks ini, perubahan konformasi sesuai dengan perubahan struktur ruang. Susunan protein didasarkan pada ikatan peptida. Jenis ikatan ini selalu menghubungkan asam amino dengan cara yang sama.
Dalam sel, ikatan peptida dimediasi oleh ribosom. Setiap ikatan peptida berhubungan dengan hubungan gugus karboksil dari satu asam amino dan gugus amino dari asam amino kedua, yang berhubungan dengan eliminasi air. Proses ini juga dikenal sebagai hidrolisis.
Dalam setiap ikatan peptida, satu ikatan menghubungkan gugus C = O dengan gugus NH. Atom nitrogen memiliki tepat satu pasangan elektron bebas. Karena elektronegativitas oksigen yang tinggi, pasangan bebas ini berada di bawah pengaruh penarikan elektron dari atom O2. Dengan cara ini, oksigen menarik sebagian pasangan elektron bebas ke dalam ikatan antara atom nitrogen dan atom karbon, dan ikatan peptida memperoleh karakter ikatan rangkap parsial. Karakter ikatan rangkap menghilangkan rotasi bebas dari gugus NH dan C = O.
Atom oksigen dan atom hidrogen dari ikatan peptida relevan untuk pembentukan struktur semua peptida dan protein tanpa kecuali. Dengan cara ini, dua asam amino dapat terikat satu sama lain. Setelah penempelan seperti itu, semua ikatan peptida dari dua rantai asam amino berhadapan langsung satu sama lain. Atom hidrogen dalam ikatan peptida relatif terpolarisasi secara positif jika dibandingkan dengan atom oksigen dalam ikatan peptida yang berhadapan langsung. Dengan cara ini, ikatan hidrogen membentuk dan menghubungkan dua rantai asam amino satu sama lain.
Semua asam amino dalam tubuh manusia adalah senyawa organik yang terdiri dari setidaknya satu gugus karboks dan satu gugus amino. Asam amino adalah komponen struktural penting dalam kehidupan manusia. Selain asam α-amino dari protein, lebih dari 400 asam amino non-proteinogenik dengan fungsi biologis diketahui tidak dapat muncul tanpa ikatan hidrogen. Gaya seperti ikatan hidrogen menstabilkan struktur tersier dari asam amino.
Anda dapat menemukan obat Anda di sini
➔ Obat untuk kelemahan ototPenyakit & penyakit
Jika ada kelainan dalam pembentukan struktur spasial protein yang fungsional, biasanya orang berbicara tentang kelainan pelipatan protein. Salah satu kondisi tersebut adalah penyakit Huntington. Penyakit genetik ini diturunkan sebagai sifat dominan autosom dan disebabkan oleh mutasi genetik pada kromosom 4. Mutasi tersebut menyebabkan ketidakstabilan produk gen. Penyakit ini merupakan penyakit neurologis yang terutama berhubungan dengan hiperkinesis tak sadar pada ekstremitas distal dan wajah. Hiperkinesis yang persisten menyebabkan kekakuan pada otot yang terkena. Selain itu, pasien dengan penyakit ini menderita peningkatan konsumsi energi.
Gejala patologis sehubungan dengan ikatan hidrogen atau struktur protein umum juga terdapat pada penyakit prion seperti penyakit sapi gila. Hipotesis paling populer adalah bahwa BSE menyebabkan kesalahan lipatan protein. Protein yang salah lipatan ini tidak dapat dipecah oleh proses fisiologis dan oleh karena itu terakumulasi di jaringan, terutama di sistem saraf pusat. Hasilnya adalah degenerasi sel saraf.
Malformasi struktur protein juga sedang dibahas dalam hubungan sebab akibat penyakit Alzheimer. Penyakit yang disebutkan tidak secara langsung mempengaruhi ikatan hidrogen, tetapi berhubungan dengan struktur spasial protein, dimana ikatan hidrogen memberikan kontribusi yang signifikan.
Organisme dengan ketidakmampuan absolut terhadap ikatan hidrogen tidak dapat hidup. Mutasi yang menyebabkan hal ini akan mengakibatkan aborsi pada awal kehamilan.












.jpg)
.jpg)